Новый пептид, полученный из матрикина, активирует гены долголетия, улучшая архитектуру внеклеточного матрикса и связи клеток кожи с матриксом
Р. Леру, К. Рингенбах, Т. Маршан, О. Пешар, П. Мондон и П. Критон
Ле-Перре-ан-Ивелин-Седекс, Франция
Абстракт
ЦЕЛЬ ИССЛЕДОВАНИЯ: Внеклеточный матрикс кожи (ВКМ) представляет собой плотную и хорошо организованную структуру, вырабатываемую фибробластами. Этот ВКМ передает механические сигналы из окружающей среды в клеточное ядро через комплекс интегрин-актин, тем самым запуская синтез белка ВКМ. Целью данного исследования было открытие нового пептида, структурно связанного с дермальными матрикинами, который способствует синтезу компонентов ECM.
МЕТОДЫ И РЕЗУЛЬТАТЫ: Были проведены скрининговые тесты со 120 пептидами с использованием нормальных дермальных фибробластов человека (крайняя плоть). В результате был выделен один представляющий интерес кандидат - ацетат N-пролилпальмитоилтрипептида-56 (PP56), который увеличивает выработку коллагена и фибронектина на генном и/или белковом уровнях. С помощью жидкостной хроматографии–тандемной масс-спектрометрии (LC-MS/МС), новейшей и инновационной аналитической технологии, в дополнение к более традиционным методам, было показано, что значительно изменяются два метаболических пути: один - для выработки коллагена, а другой - актина.
РЕЗУЛЬТАТЫ: Результаты показали, что этот пептид является потенциальным кандидатом для улучшения плотности и организации ВКМ новым способом.
Вступление
Гомеостаз тканей контролируется взаимодействиями между клетками и внеклеточным матриксом. Клетки вырабатывают окружающий их внеклеточный матрикс (ВКМ), который связывает их вместе, предоставляя информацию о пространственном местоположении, подавая сигналы прикрепления, размножения, способствуя синтезу и передавая механические сигналы окружающей среды. Сильные взаимодействия между клетками и матриксом иллюстрируются работами, показывающими, что у молодых клеток, включенных в старый и поврежденный матрикс, синтез был снижен, в то время как у клеток пожилого человека синтез матрикса возобновлялся, когда они были включены в молодой матрикс. Таким образом, качество матрицы изменяет поведение клеток.
Дермальный ВКМ - это сложная трехмерная сеть, включающая в себя несколько взаимодействующих молекул, таких как коллаген-I, коллаген-III, коллаген-IV, коллаген-VI и фибронектин. Выработка зрелого фибриллярного коллагена-I - это сложный механизм, состоящий из нескольких этапов, которые находятся под контролем группы ферментов, участвующих в выработке и созревании коллагена или в его отложении.
Хорошо известно, что выработка некоторых коллагенов изменяется с возрастом и под воздействием фотоэкспозиции; следовательно, это ухудшает качество дермального ВКМ. Кроме того, нарушение работы нефибриллярного коллагена VI приводит к истончению дермы из-за уменьшения его свойств организатора ВКМ, снижению выработки коллагена и протеогликанов и отложению фибронектина. Таким образом, улучшение качества ВКМ и производства его белков представляет интерес для борьбы со старением и повреждениями кожи.
Фибронектин - это гликопротеин, связывающий несколько белков ВКМ (коллагены, протеогликаны, фибронектин и т.д.) и интегрины клетки благодаря сложному белку, состоящему из интегринов, α-актинина, талина и актино (рис. 1). Внешнее напряжение воздействует на эту взаимосвязанную сеть и запускает каскады клеточного фосфорилирования, приводящие к перестройке актинового цитоскелета.
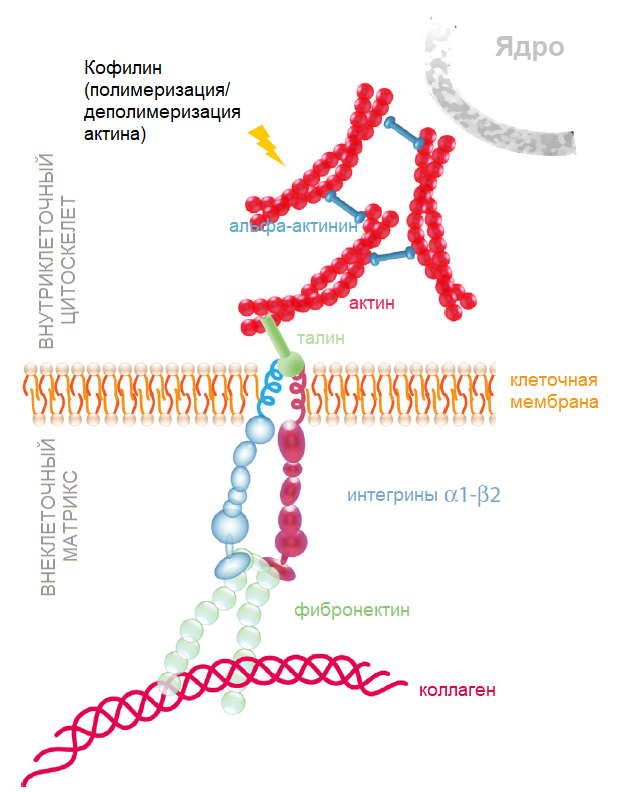
Рисунок 1. Закрепляющий комплекс между актиновым цитоскелетом и внеклеточным матриксом посредством талина, α-актинина и фибронектина.
Пептид PP56 (N-пролилпальмитоиллизилгистидилглицин, CAS: 1899049-18-3) был синтезирован с помощью смешанного твердофазного/жидкофазного синтеза (рис. 2). Для исследований на культуре клеток использовали модифицированную среду Eagle (DMEM), разработанную компанией Dulbecco, эмбриональную телячью сыворотку (FCS), пенициллин–стрептомицин (10 000 МЕ/мл пенициллина и 10 мг/мл стрептомицина) и физиологический раствор с фосфатным буфером (PBS) (Gibco, Thermo Fisher ScientificTM, США). Первичные клетки дермальных фибробластов человека были выделены из образцов крайней плоти человека и предоставлены компанией Cambrex™
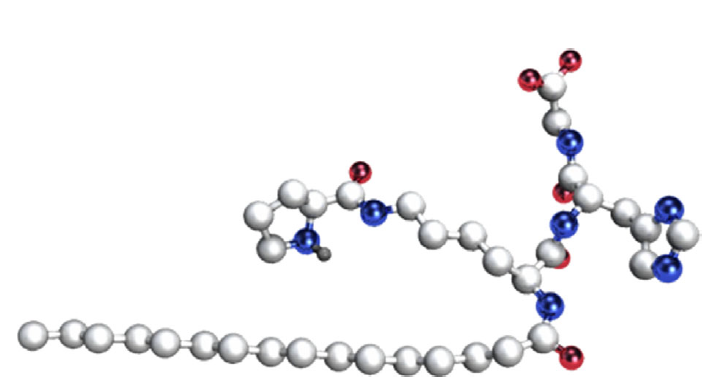
Рисунок 2. 3D cтруктура PP56
Для ежедневного содержания клетки высевали в колбу объемом 175 см2 в среде DMEM с добавлением 10% FCS, 100 ЕД/мл пенициллина, 100 мг/мл стрептомицина и 1% об/об L-глютамина и инкубировали при 37°C в увлажненной 5%-ной атмосфере CO2. Среду обновляли каждые 48 ч, чтобы обеспечить рост крайней плоти. Во всех последующих экспериментах крайнюю плоть использовали между 4-м и 12-м пассажами в зависимости от проводимого анализа. Слои крайней плоти были диссоциированы с использованием трипсина и посеяны на тестовую подложку, такую как чашки Петри или в DMEM с добавлением 10% FCS.
Послеконтакта пептида с клетками и промывки клеточного слоя были проведены протеомные исследования методом спектрометрии на экстрактах крайней плоти, белки которых были предварительно обработаны трипсином для получения пептидных фрагментов.
Для иммуногистологических исследований были использованы кожные эксплантаты человека (Эквивалент человеческой кожи, брюшная полость, женщина, 33 года, европеоид, BiopredicTM, Франция) с питательной средой (BIO-ECTM, Франция). Кремы, содержащие 10 частей на миллион PP56, или крем-плацебо наносили местно один раз в день в течение 6 дней. Затем были проведены иммуногистологические исследования срезов (7 мкм, Leica, Германия), нацеленных на белок талин.
Результаты
На культурах крайней плоти 2D для обнаружения нового пептида были проведены скрининговые тесты. После контакта с пептидами (0,1–100 частей на миллион) были использованы ИФА и ммуноцитохимические тесты, для оценки и сравнения продукции коллагена-I, коллагена-IV и фибронектина этими пептидами. Результаты показали, что PP56 был лучшим кандидатом, значительно повышающим эффективность всех этих препаратов. Это соединение было выбрано для дальнейших исследований.
Что касается перекрестного взаимодействия между клеткой и ВКМ, мы наблюдали, что выработка двух связанных с актином белков, a-актинина и кофилина, значительно увеличилась при использовании PP56 на 82% и 95% соответственно по сравнению с контролем. Затем иммуноцитохимические исследования показали, что PP56 усиливает сигналы актина и кофилина при СН по сравнению с контролем (92,87 и 95,46, оба Р < 0,01, рис. 3). Иммуногистологические исследования, проведенные в HSE, показали, что уровень талина был значительно повышен на 66% (Р < 0,01).
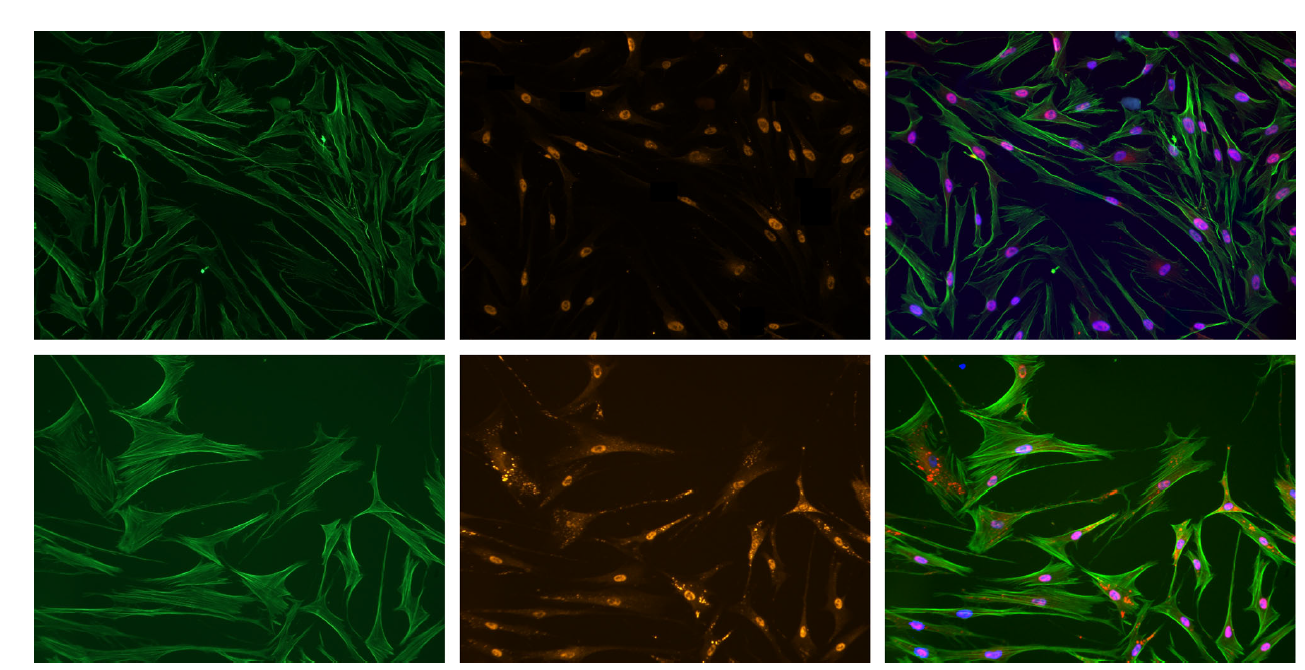
Рисунок 3. Визуализация изменения содержания актина (зеленый) и кофилина (оранжевый) в HF без (верхние изображения) или с PP56 (нижние изображения); изображения справа являются объединенными изображениями. n = 3.
Интересно, что в дополнение к увеличению количества коллагенов и их качества, происходит увеличение выработки фибронектина и коллагена-VI, двух известных белков, участвующих в формировании коллагеновой сети. Действительно, без того или иного из них дерма менее хорошо организована, а образование зрелого коллагена сильно нарушено. Оригинальный способ визуализации качества архитектуры матричной сети (как с точки зрения количества, так и сложности) заключается в поиске основных векторов зрелых волокон на фотографиях в исследовании (рис. 5). С помощью этого метода можно сразу увидеть сложность сети, которая, является более плотной.
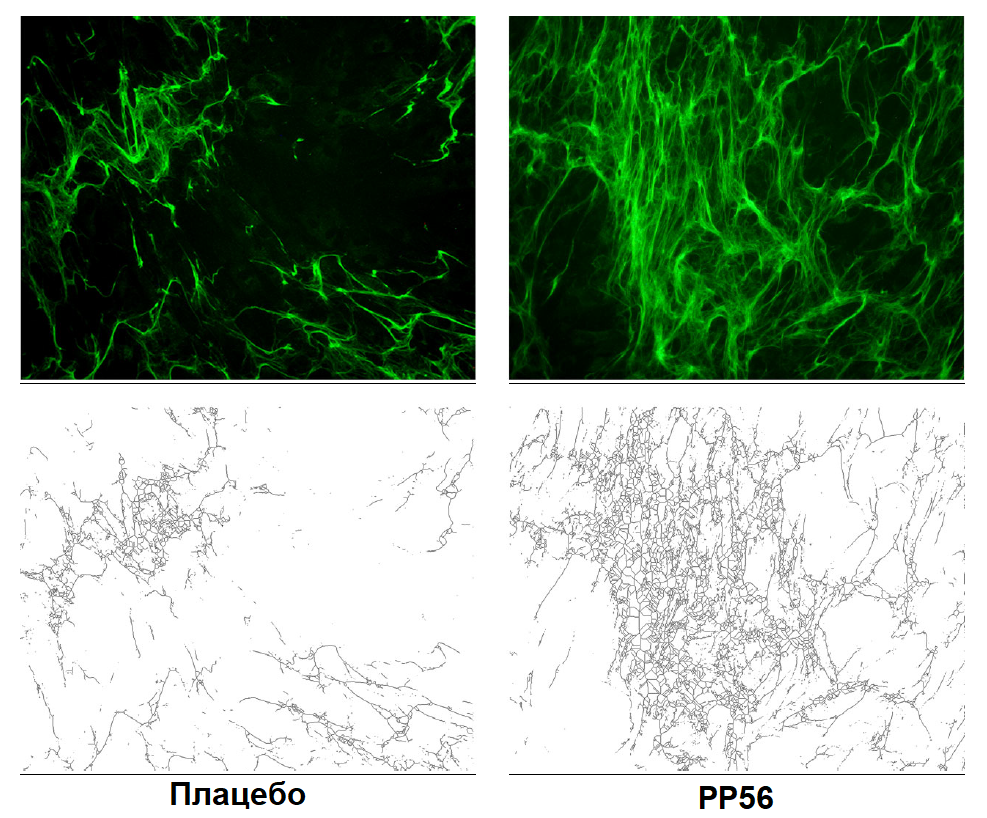
Рисунок 5. Визуализация сложности и уплотнения коллагеновой сети I типа. Влияние PP56 на фибробласты (×200).