Нури О, Джуен Хван, Мун Сон Кан, Чон Юль Ю, Минсок Квак и Дон Ук Хан
Химико-биологический факультет Корейской академии наук Корейского института передовых наук и технологий. Пусан, 47162, Республика Корея.
Химический факультет Национального университета Пукёнг. Пусан, 48513, Республика Корея.
Центр трансляционных исследований для активных старшеклассников на базе Smart Gym.
Здравоохранение, Национальный университет Пукёнг, Пусан, 48513, Республика Корея. *
Научно-исследовательский центр энергетики Аджу, Университет Аджу. Сувон, 16499, Республика Корея.
Научно-исследовательский институт механических технологий. Пусанский национальный университет. Пусан, 46241, Республика Корея.
Факультет исследований энергетических систем и химии. Университет Аджу, Сувон, 16499. Республика Корея.
Индустрия конвергентной бионики для индустрии 4.0. Национальный университет Пукёнг. Пусан, 48513, Республика Корея.
Факультет когнитивно-мехатронной инженерии, Пусанский национальный университет. Пусан, 46241, Республика Корея.
Институт нано-биоконвергенции Пусанского национального университета. Пусан, 46241, Республика Корея.
Основной механизм ПДРН для регенерации тканей.
За последнее десятилетие значительное внимание было уделено полидезоксирибонуклеотиду (ПДРН) из-за его многообещающих фармакологических свойств, соответственно, целью данной статьи является обзор и обобщение последних экспериментальных исследований ПДРН в области тканевой инженерии и регенерации. Представлены уникальные биохимические механизмы ПДРН, способствующие послушности клеток и регенерации. Классифицируются такие широко используемые области тканной инженерии на основе ПДРН, как регенерация нервно-мышечных тканей, диабетических ран или кожи, а также костей.
Эффекты ПДРН, вызывающие пролиферацию.
Кратко описаны процесс деградации и специфические сигнальные пути ПДРН для пролиферации, иммуномодуляции и дифференцировки в зависимости от специфических линий (например, миогенеза, нейрогенеза, заживления ран и остеогенеза). ПДРН расщепляется активными ферментами клеточной мембраны, обеспечивая обильный источник дезоксинуклеотидов и дезоксинуклеозидного ряда. Продемонстрировано, что ПДРН значительно стимулирует пролиферацию остеобластов человека, демонстрируя максимальное увеличение на 21% после 6 дней in vitro. Добавление 3,7-диметил-1-пропаргилксантина (DMPX, пуринергического ингибитора A2AR) к обработанным ПДРН клетки индуцировало снижение клеточной пролиферации на 42,9% через 6 дней по сравнению с клетками, обработанными только ПДРН, что позволяет предположить, что путь A2AR не является единственным путем, но играет важную роль в пролиферации клеток, индуцированной ПДРН. Показано, что активация A2AR CGS21680 (агонистом) способствует пролиферации в линиях клеток рака легкого A549, молочной железы MRMT-1 и меланомы A375.
Регенерация и омоложение кожи с помощью ПДРН или ПН
ПДРН и ПН, оба соединения, полученные из ДНК, продемонстрировали значительный потенциал в регенерации и омоложении кожи благодаря их способности стимулировать восстановление клеток и регенерацию тканей (таблица S4). Стимулируя активность фибробластов, синтез коллагена и ангиогенез, ПДРН и ПН эффективно восстанавливают кожу, улучшают текстуру и эластичность, а также уменьшают видимые признаки старения, такие как морщины. Большинство исследований посвящено влиянию ПДРН на регенерацию кожи, основное внимание уделялось моделям клеток фибробластов. Однако физиологическое заживление ран представляет собой сложный процесс, включающий взаимодействие между клетками воспаления, фибробластами, кератиноцитами, эндотелиальными клетками, факторами роста и ферментами. ПДРН не только усиливает пролиферацию и миграцию клеток, но и способствует накоплению коллагена, который необходим для противодействия деградации коллагена и образованию морщин в процессе старения. Фотостарение, основная причина появления морщин, обусловлено изменениями коллагена. В то же время ультрафиолетовое излучение вызывает разрушение матрикса синтез металлопротеиназы (ММР), приводящий к повреждению соединительной ткани в результате опосредованного ММР разрушения коллагена и последующего старения кожи.
В одном из исследований был приготовлен сшитый гидрогель ГК-ПДРН (ГП) посредством ковалентного взаимодействия между карбоксильными группами ГК и аминогруппами ПДРН в присутствии 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния хлорида (DMTMM). (Рис. 4А). Оптимизированный состав, содержащий 0,6% HA и 0,5% ПДРН, обладает повышенной механической прочностью и стабильностью благодаря повышенной плотности сшивок, что способствует его длительному биологическому разложению in vivo. Этот препарат не вызывал воспалительной реакции, в то время как инкапсуляция фиброза и ангиогенез постепенно уменьшались, со временем это сопровождается усиленной пролиферацией фибробластов и отложением межклеточного вещества, тем самым укрепляя структурную целостность гидрогеля (рис. 4B). По сравнению с гидрогелем ГК, сшитый гидрогель ГК способствует синтезу коллагена и укрепляет пучки коллагеновых волокон, эффективно стимулируя рост фибробластов для регенерации кожи, обеспечивая при этом повышенную стабильность объема и механическую поддержку. Кроме того, применение ПДРН сыграло решающую роль в модулировании деградации гидрогеля, обеспечивая контролируемое разрушение и длительную биологическую активность. Дополнительно, сшитый гидрогель ГП также подавлял экспрессию потенциального ваниллоидного рецептора 4 (TRPV4), проницаемого для кальция катионного канала, связанного с экспрессией ММР и воспалительных цитокинов при раздражении кожи, тем самым смягчая воспалительные реакции и способствуя замедлению старения кожи (рис. 4В).
Рис. 4. Сшитый гидрогель с гиалуроновой кислотой (ГК) и ПДРН (ГП) для регенерации кожи. (А) Процесс изготовления и морфология сшитого гидрогеля ГП. (В) Оценка синтеза коллагена с течением времени, визуализируемая с помощью окрашивания Sirius Red, через 2, 4, 8, 16 и 24 недели после лечения гидрогелем ГК и гидрогелем ГП. (C) Сравнительный анализ экспрессии транзиторного рецепторного потенциала ваниллоида 4 (TRPV4) в тканях мыши после обработки гидрогелем ГК и гидрогелем ГП, оцененный с помощью иммунофлуоресцентного окрашивания. DMTMM, 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния хлорид.
Химико-биологический факультет Корейской академии наук Корейского института передовых наук и технологий. Пусан, 47162, Республика Корея.
Химический факультет Национального университета Пукёнг. Пусан, 48513, Республика Корея.
Центр трансляционных исследований для активных старшеклассников на базе Smart Gym.
Здравоохранение, Национальный университет Пукёнг, Пусан, 48513, Республика Корея. *
Научно-исследовательский центр энергетики Аджу, Университет Аджу. Сувон, 16499, Республика Корея.
Научно-исследовательский институт механических технологий. Пусанский национальный университет. Пусан, 46241, Республика Корея.
Факультет исследований энергетических систем и химии. Университет Аджу, Сувон, 16499. Республика Корея.
Индустрия конвергентной бионики для индустрии 4.0. Национальный университет Пукёнг. Пусан, 48513, Республика Корея.
Факультет когнитивно-мехатронной инженерии, Пусанский национальный университет. Пусан, 46241, Республика Корея.
Институт нано-биоконвергенции Пусанского национального университета. Пусан, 46241, Республика Корея.
Основной механизм ПДРН для регенерации тканей.
За последнее десятилетие значительное внимание было уделено полидезоксирибонуклеотиду (ПДРН) из-за его многообещающих фармакологических свойств, соответственно, целью данной статьи является обзор и обобщение последних экспериментальных исследований ПДРН в области тканевой инженерии и регенерации. Представлены уникальные биохимические механизмы ПДРН, способствующие послушности клеток и регенерации. Классифицируются такие широко используемые области тканной инженерии на основе ПДРН, как регенерация нервно-мышечных тканей, диабетических ран или кожи, а также костей.
Эффекты ПДРН, вызывающие пролиферацию.
Кратко описаны процесс деградации и специфические сигнальные пути ПДРН для пролиферации, иммуномодуляции и дифференцировки в зависимости от специфических линий (например, миогенеза, нейрогенеза, заживления ран и остеогенеза). ПДРН расщепляется активными ферментами клеточной мембраны, обеспечивая обильный источник дезоксинуклеотидов и дезоксинуклеозидного ряда. Продемонстрировано, что ПДРН значительно стимулирует пролиферацию остеобластов человека, демонстрируя максимальное увеличение на 21% после 6 дней in vitro. Добавление 3,7-диметил-1-пропаргилксантина (DMPX, пуринергического ингибитора A2AR) к обработанным ПДРН клетки индуцировало снижение клеточной пролиферации на 42,9% через 6 дней по сравнению с клетками, обработанными только ПДРН, что позволяет предположить, что путь A2AR не является единственным путем, но играет важную роль в пролиферации клеток, индуцированной ПДРН. Показано, что активация A2AR CGS21680 (агонистом) способствует пролиферации в линиях клеток рака легкого A549, молочной железы MRMT-1 и меланомы A375.
Регенерация и омоложение кожи с помощью ПДРН или ПН
ПДРН и ПН, оба соединения, полученные из ДНК, продемонстрировали значительный потенциал в регенерации и омоложении кожи благодаря их способности стимулировать восстановление клеток и регенерацию тканей (таблица S4). Стимулируя активность фибробластов, синтез коллагена и ангиогенез, ПДРН и ПН эффективно восстанавливают кожу, улучшают текстуру и эластичность, а также уменьшают видимые признаки старения, такие как морщины. Большинство исследований посвящено влиянию ПДРН на регенерацию кожи, основное внимание уделялось моделям клеток фибробластов. Однако физиологическое заживление ран представляет собой сложный процесс, включающий взаимодействие между клетками воспаления, фибробластами, кератиноцитами, эндотелиальными клетками, факторами роста и ферментами. ПДРН не только усиливает пролиферацию и миграцию клеток, но и способствует накоплению коллагена, который необходим для противодействия деградации коллагена и образованию морщин в процессе старения. Фотостарение, основная причина появления морщин, обусловлено изменениями коллагена. В то же время ультрафиолетовое излучение вызывает разрушение матрикса синтез металлопротеиназы (ММР), приводящий к повреждению соединительной ткани в результате опосредованного ММР разрушения коллагена и последующего старения кожи.
В одном из исследований был приготовлен сшитый гидрогель ГК-ПДРН (ГП) посредством ковалентного взаимодействия между карбоксильными группами ГК и аминогруппами ПДРН в присутствии 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния хлорида (DMTMM). (Рис. 4А). Оптимизированный состав, содержащий 0,6% HA и 0,5% ПДРН, обладает повышенной механической прочностью и стабильностью благодаря повышенной плотности сшивок, что способствует его длительному биологическому разложению in vivo. Этот препарат не вызывал воспалительной реакции, в то время как инкапсуляция фиброза и ангиогенез постепенно уменьшались, со временем это сопровождается усиленной пролиферацией фибробластов и отложением межклеточного вещества, тем самым укрепляя структурную целостность гидрогеля (рис. 4B). По сравнению с гидрогелем ГК, сшитый гидрогель ГК способствует синтезу коллагена и укрепляет пучки коллагеновых волокон, эффективно стимулируя рост фибробластов для регенерации кожи, обеспечивая при этом повышенную стабильность объема и механическую поддержку. Кроме того, применение ПДРН сыграло решающую роль в модулировании деградации гидрогеля, обеспечивая контролируемое разрушение и длительную биологическую активность. Дополнительно, сшитый гидрогель ГП также подавлял экспрессию потенциального ваниллоидного рецептора 4 (TRPV4), проницаемого для кальция катионного канала, связанного с экспрессией ММР и воспалительных цитокинов при раздражении кожи, тем самым смягчая воспалительные реакции и способствуя замедлению старения кожи (рис. 4В).
Рис. 4. Сшитый гидрогель с гиалуроновой кислотой (ГК) и ПДРН (ГП) для регенерации кожи. (А) Процесс изготовления и морфология сшитого гидрогеля ГП. (В) Оценка синтеза коллагена с течением времени, визуализируемая с помощью окрашивания Sirius Red, через 2, 4, 8, 16 и 24 недели после лечения гидрогелем ГК и гидрогелем ГП. (C) Сравнительный анализ экспрессии транзиторного рецепторного потенциала ваниллоида 4 (TRPV4) в тканях мыши после обработки гидрогелем ГК и гидрогелем ГП, оцененный с помощью иммунофлуоресцентного окрашивания. DMTMM, 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния хлорид.
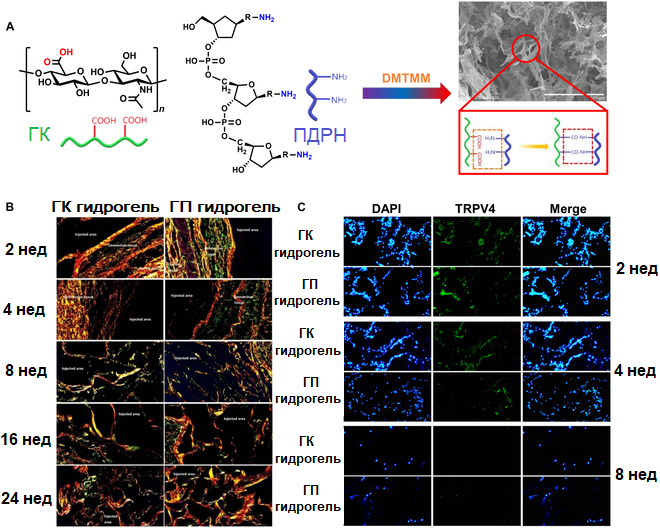
Table S4. Таблица S4. Стратегия и эффект применения материалов с использованием PDRN или PN complex для регенерации кожи